美國藥廠Regeneron Pharmaceuticals 表示,將與美國食品及藥物管理局(FDA)共享數據,並要求擴大緊急用途的使用範圍,批准旗下新冠治療藥作預防治療用途。
根據 美國食品藥品監督管理局(FDA)授權的緊急用途 (EUA) ,REGEN-COV目前在美國可用於治療成年人以及至少12歲以上的小兒患者和成人的輕度至中度感染新冠病毒。體重至少40公斤,已獲得直接新冠病毒檢測的陽性結果,並有發展為嚴重新冠和/或住院的高風險。REGEN-COV尚未獲得FDA的批准,但已被授權用於緊急情況。
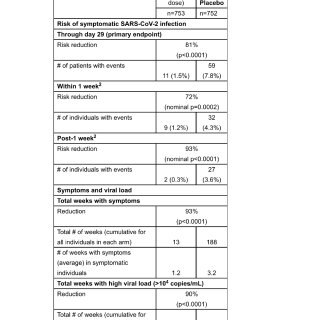
Regeneron表示,研究邀請1,505名未受感染但同區出現確診個案的人士參與,參加試驗的人中有41%為拉丁裔、9%為黑人,33%有肥胖症,肥胖者中33%且年齡在50歲以下(中位年齡:44歲;範圍:12-92歲)的肥胖者佔38%。於美國進行的第三階段臨床測試中顯示,該藥可將個人症狀性感染的風險降低81%。有症狀並接受過這種藥物治療的人比使用安慰劑的人平均症狀緩解了兩周。表明REGEN-COV在預防新冠感染者的家庭接觸中預防症狀性COVID-19方面非常有效‼️
Regeneron的療法是被稱為單克隆抗體的一類療法的一部分,這種單克隆抗體可起到免疫細胞和抵抗感染的作用。在特朗普於十月份收到再生元的藥物的消息傳出後,單克隆抗體治療獲得了廣泛的關注。
✳️資料來源於CNBC & Regeneron Pharmaceuticals